Actas XXII Foro Nacional de Ovino 2020 1ª Ponencia Seminario 1: Las vacunas: la clave de la prevención en ovino
Desarrollo de una vacuna: desde la idea hasta el producto
Carlos Montbrau1 y Mireia Fontseca2
1Investigador I+D en HIPRA
2Investigador-gestor I+D en HIPRA
27/10/2020En el mejor de los escenarios, una vacuna se puede desarrollar en cinco años, aunque si hay complicaciones puede durar más de diez. De promedio en HIPRA estamos en torno a los 8 años. Sin embargo, como ha sucedido con el COVID-19, en situaciones de emergencia sanitaria se permiten registros condicionales. Para ello, se debe realizar una declaración de emergencia sanitaria en un país o países y estas autoridades marcan unos requisitos mínimos. La documentación debe tener la misma calidad que en un registro convencional, pero se permite iniciar el registro aportando una parte de las pruebas convencionales, con el compromiso de completar toda la información (resto de pruebas) al finalizar la licencia condicional. El limitante es que se obtiene el registro en esos países que han declarado la emergencia, esa licencia condicional sólo se tiene durante un periodo determinado.


Fase 0: Definición del producto
Posteriormente, se comienza con la búsqueda de los candidatos vacunales (los antígenos). Los antígenos pueden ser de diferentes clases, pueden ser microorganismos completos (vivos atenuados o inactivados), subunidades o fracciones (obtenidos de forma natural o mediante ingeniería genética), vectores vacunales (portadores de otros antígenos) y vacunas de DNA.
Centrándonos en las vacunas más habituales, por un lado, tenemos las vacunas vivas atenuadas. Vacunas potentes. Inducen inmunidad celular y humoral, por lo que es posible que no precisen de adyuvante. Son baratas de producir y no siempre es necesaria una dosis de recuerdo. Estas vacunas pueden tener una virulencia residual e incluso puede revertir su atenuación y provocar la enfermedad.
Por otro lado, tenemos las vacunas inactivadas. Vacunas seguras y estables. Inducen principalmente una inmunidad humoral. En estas vacunas el antígeno no replica dentro del organismo y puede que la inmunidad que se genere no sea completa, aunque se tienen soluciones farmacológicas para solucionarlo, los adyuvantes, que ayudan a potenciar esta inmunidad. Estas vacunas suelen precisar de dosis de recuerdo y son más caras de producir. Las vacunas inactivadas pueden tener interferencia antigénica.
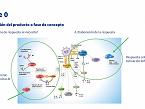
Finalmente, se estudia la respuesta inmunológica de la vacuna. El sistema inmunitario tiene unas células llamadas APC (Células presentadoras de antígenos), como suelen ser los macrófagos y las células dendríticas, que se encargan de identificar el patógeno. Estas células tienen unos receptores de reconocimiento (PRR), que permiten el reconocimiento de los patrones moleculares que tienen los patógenos (PAMP). Cuando este reconocimiento se realiza, se empieza a generar toda una cascada de señal. En función de si el patógeno o antígeno que ha entrado es un virus, una bacteria, una toxina o un parásito, la respuesta que se genera es distinta. Si el patógeno o antígeno es una bacteria, la inmunidad que se prioriza es una activación de los linfocitos B que inducirán la producción de anticuerpos promoviendo una respuesta más de tipo humoral. Si es un virus, una bacteria intracelular o un parásito, la respuesta que se genera es más de tipo celular, por lo que se activan los linfocitos T CD8. Lo importante es generar una buena memoria inmunológica, que es la propiedad que tiene el sistema inmune para recordar los antígenos con los que ya ha estado en contacto anteriormente y desencadenar una respuesta mucho más rápida y más efectiva. Por lo tanto, la memoria inmunológica es la base de la vacunación.
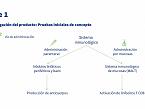
Fase 1: Definir composición, vía y plan de vacunación
En la actualidad, se están investigando otras vías de administración a través de las mucosas, que activan el sistema MALT y los linfocitos TCD8. Serían las vías intranasal u oral.
Una vez se ha determinado la vía de administración, se analiza el plan de administración de acuerdo con las condiciones de campo y se prueban distintas dosis de la vacuna para determinar la mínima dosis eficaz. Finalmente, también se elige el adyuvante más adecuado. Cuando se administra una vacuna que tiene adyuvante, se incrementa la migración de las células presentadoras de antígeno en el punto de inoculación, se incrementa su eficiencia y potencia su maduración. Por último, se puede promover la inmunidad celular y una liberación prolongada del antígeno. El adyuvante debe ser puro, no tóxico, proporcionar una memoria a largo plazo, no tener efectos indeseados, estable en tiempo, temperatura y pH y biodegradable.
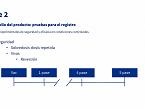
Fase 2: Establecer seguridad y eficacia de la vacuna
Las pruebas de seguridad se realizan con vacunas con una mayor carga de antígeno y adyuvante de la que se acabará comercializando. Son más potentes para tener clara su seguridad. Una de las pruebas que se realiza, tanto en vacunas vivas como inactivadas, es la prueba de sobredosis y dosis repetida. Tomando como ejemplo una vacuna cuyo plan de administración sean dos dosis separadas por 21 días, en esta prueba se da una sobredosis de vacuna que suele ser diez o dos veces más de lo que se administraría de forma convencional, seguido de una segunda administración normal a los 21 días y, por último, una dosis adicional (o repetida) 21 días después. Desde la administración de la primera sobredosis hasta 28 días después de la última dosis adicional, se monitorizan los animales para observar si existen reacciones locales y generales. En el caso de que existan, que sean lo más leves posibles. De esta forma, se asegura que, si en campo se administra una sobredosis o una dosis no necesaria, las reacciones que se observarían serían inexistentes o leves. Para las vacunas vivas, se requieren pruebas específicas. Estas vacunas siempre parten de una cepa original atenuada, que se guarda en stock. Esta cepa madre es la que se utiliza para realizar estas pruebas. Se trata de una cepa menos manipulada y con más título, precisamente para poner a la vacuna en la peor circunstancia.
Con esta vacuna se testará la reversión, es decir, que no se vuelva virulenta al pasar a animales. Por lo tanto, se vacunan animales y se recogen muestras para detectar si hay virus vivo. Si lo hay, se pasa a otro grupo de animales y se vuelven a recoger. Así sucesivamente durante cinco grupos. Durante todo este tiempo se monitoriza que no aparezcan signos clínicos o, si ya existen desde la primera vacunación porque es una vacuna que induce ciertos signos clínicos, que no sean más graves. Se compara la vacuna con el quinto pase para comprobar que la vacuna atenuada no se ha vuelto virulenta.
En la prueba de diseminación, también requerida en vacunas vivas, se vacuna a una serie de animales y se sacrifican al cabo de pocos días: cuatro, ocho o doce días. Se toman muestras de tejido de distintas partes para determinar cómo replica y disemina dentro del organismo del animal. Siempre se hace teniendo en cuenta los requisitos de las autoridades, pero en algunos casos se ha comprobado que pueden acantonarse y no se podría comprobar en estas pruebas.
Por último, está la prueba de excreción. Se toman una serie de animales vacunados y se mezclan con otros sin vacunar. Se analiza la capacidad infectiva que tendría la vacuna sobre los nos vacunados.
También tanto para vacunas vivas como para inactivadas se evalúa la seguridad en diferentes categorías de animales, como gestantes, lactantes Estas pruebas no son requeridas por las autoridades, pero son necesarias si se quiere tener una mayor practicidad para el ganadero.
Respecto a la eficacia de la vacuna, existen varios tipos de pruebas. Una de ellas es la de inicio de inmunidad, que se trata de demostrar a partir de qué día después de la vacunación es eficaz la inmunidad. Para ello se usan dos grupos de animales, unos vacunados y otros control. Después se realiza una infección experimental tan temprano como se crea que la vacuna puede ser eficaz. En algunos casos, se puede demostrar eficacia antes de que se vea respuesta serológica evidente. La seroconversión es importante, pero es más decisiva la eficacia ante una infección experimental, que es lo que da la calidad de la vacuna. Normalmente la infección experimental es más adversa de lo que se vivirá en campo, por lo que si hay eficacia en ese momento, en campo debería ser mayor.
Otro aspecto que se debe valorar es la interferencia de los anticuerpos maternales. Esta prueba sólo se debe hacer en aquellos casos que se realizan vacunaciones tempranas. En ovino se vacunan madres gestantes y se transfiere a un calostro que es capaz de proteger durante dos o tres meses de vida. Este hecho es muy variable en función de los patógenos. Si la vacuna se va a administrar antes de los cuatro o cinco meses de vida del animal, sí sería necesaria llevar esa prueba. Se testan cuatro grupos: uno vacunado y otro control con anticuerpos maternales y otro vacunado y control que no tienen anticuerpos frente al patógeno de estudio. Estos cuatro grupos reciben la vacuna o el placebo y la infección se lleva a cabo cuando el grupo control que tenía anticuerpos maternales pierde esta protección. Se comprueba la eficacia de la vacuna y que la vacuna no haya perdido eficacia por influencia de los anticuerpos maternales. Esta prueba es muy importante principalmente en las vacunas vivas, porque los anticuerpos maternales pueden anular o disminuir la capacidad de generar inmunidad de la vacuna, por lo que pierde eficacia y duración de la eficacia.
También se hace una prueba de duración de la inmunidad, infectando tan lejos como se crea que la vacuna sigue siendo eficaz. Esta prueba determina la memoria inmunitaria que induce la vacuna. Algunas vacunas que tienen varias valencias pueden tener duraciones inmunitarias diferentes. Por ejemplo, una valencia puede tener una vigencia de seis meses y otra de doce meses. Por lo tanto, si se hacen vacunaciones anuales, puede ser que la memoria inmunológica de la valencia de seis meses se haya perdido. La prueba booster o dosis de recuerdo sirve para saber el momento en el que se debe administrar esa dosis. La duración de la inmunidad generada con la dosis de recuerdo puede ser mayor que la obtenida en el plan vacunal inicial. Esto sucede gracias a la memoria inmunogénica. Después de una primera vacunación, hay una inducción de anticuerpos y se genera una memoria inmunogénica. Cuando se entra en contacto con el patógeno o con otra dosis de la vacuna, ésta induce una gran subida de anticuerpos, que prolonga la memoria inmunogénica. Es importante no esperar demasiado para que no se pierdan los efectos de la primera vacunación.
Fase 3: Evaluación del producto en campo
Se podrán testar diferentes planes vacunales en diferentes edades. Se puede aplicar en un gran número de animales y en explotaciones ya seleccionadas. Se buscan granjas que hayan tenido problemas con el patógeno o que se espere una incidencia alta, con el objetivo de demostrar la eficacia en condiciones de campo.
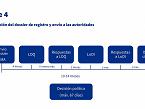
Fase 4: Proceso de registro
Todo lo que aparece en el prospecto debe poder demostrarse de una forma muy precisa. Ante la falta de pruebas, las autoridades lo descartan. Por ejemplo, se puede demostrar que una vacuna es segura y eficaz en animales de tres meses y se han realizado todas las pruebas en animales de tres meses, pero en una de ellas había animales de cuatro meses, por lo que el prospecto señalaría que sólo es eficaz desde los cuatro meses de edad. Por lo tanto, son muy estrictos.
Tras el último envío de preguntas de la Agencia del Medicamento, hay un mes para responder a esas preguntas y se debe esperar un mes más para tener una decisión científica. Al cabo de dos meses llega una decisión política que permite la producción.
Conclusiones
- Para desarrollar una vacuna se requiere de mucho tiempo dedicado, mucha resiliencia y mucha dedicación de personas y recursos.
- El conocimiento es muy importante. No es lo mismo partir de cero, qué conociendo muchos conceptos ligados al patógeno y al desarrollo vacunal. En HIPRA sólo se desarrollan nuevas vacunas, nos hemos centrado en la prevención y eso nos ha dado mucho conocimiento en diversos proyectos. Con este conocimiento se evitan o reducen diversos problemas que ya han surgido previamente en otros proyectos.
- Hay muchos factores que afectan a la inmunología. Todos ellos se tienen en cuenta, en la medida de lo posible, en el desarrollo de la vacuna. Se intenta desarrollar el producto más versátil y adaptable a las condiciones de campo.